ゲノム編集・遺伝子編集が日常を変える時代はすでに到来しています。私たちの日常とは関わりの少ない最先端技術といった印象を持っている人も多いかもしれませんが、実は私たちの健康や食の未来は、ゲノム編集や遺伝子編集の技術と無関係ではありません。
私たちの生活を豊かにする大きな可能性を秘めた、ゲノム編集がもたらす医療でのメリットや、食料生産での活用事例、知っておくべきデメリット、倫理的な課題まで、わかりやすく解説します。
目次
ゲノム編集・遺伝子編集とは
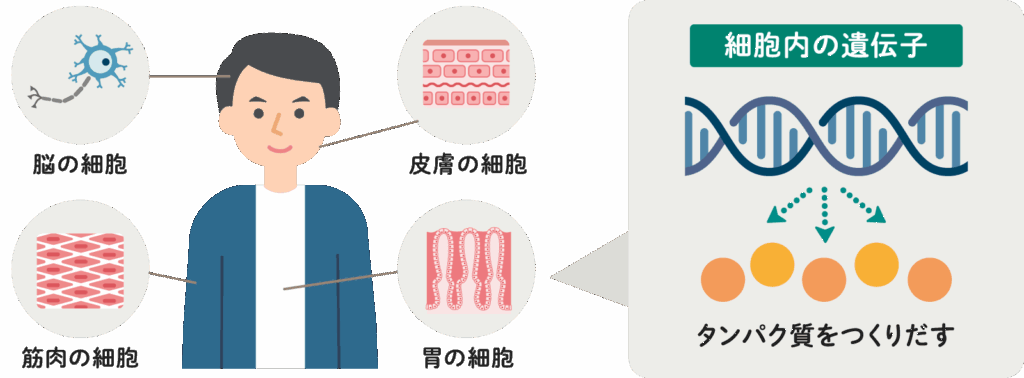
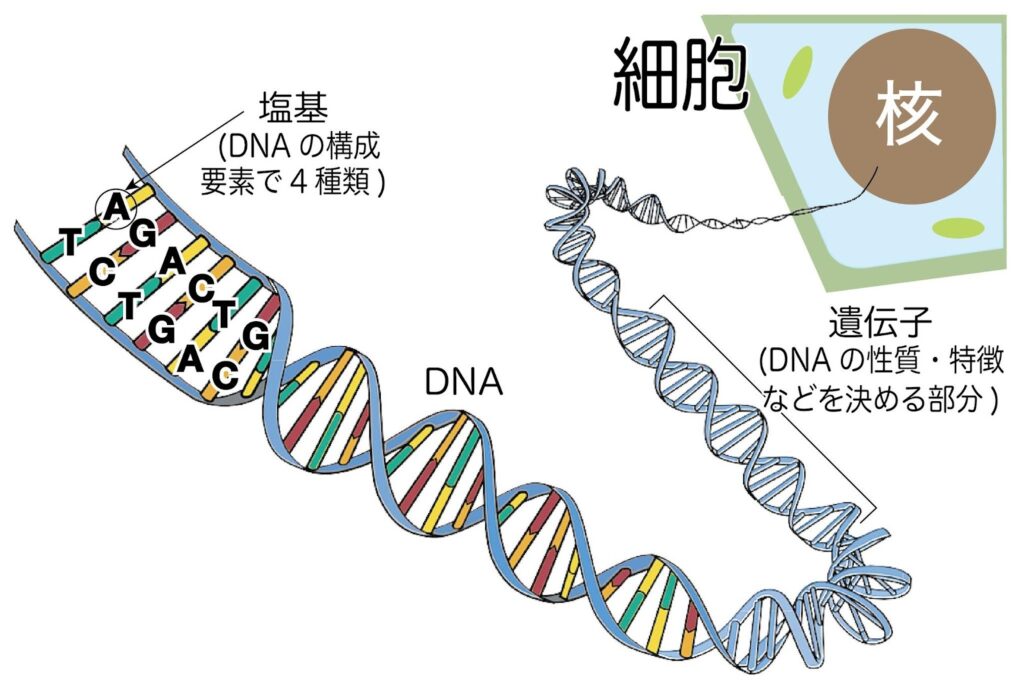
私たちの体は、およそ37兆個の細胞からできています。そのすべての細胞の中にある設計図が「DNA」であり、DNAの中で特定の性質や働きを決める単位が「遺伝子」です。
これらの遺伝子が多数集まって構成されている全体像を「ゲノム」と呼びます。遺伝子編集やゲノム編集とは、この設計図に意図的に手を加える技術です。
病気の治療や農作物の改良、環境への応用など、医療・農業・バイオ産業においてこの技術の可能性は急速に広がっていますが、同時に倫理的・社会的な課題も問われています。また、ゲノム編集と遺伝子編集は、よく似た用語として扱われますが、実は意味や指す範囲に違いがあります。
まずは両者の違いなど、基本的なことを明確にしておきましょう。
遺伝子・ゲノム・DNAの関係性
【遺伝子とは】
生命の現象を理解する上で欠かせない三つの重要な言葉があります。
- DNA
- ゲノム
- 遺伝子
これらは密接に関連しながらも、それぞれ異なる階層の概念を示しています。
①DNA(デオキシリボ核酸)
【DNAとは】
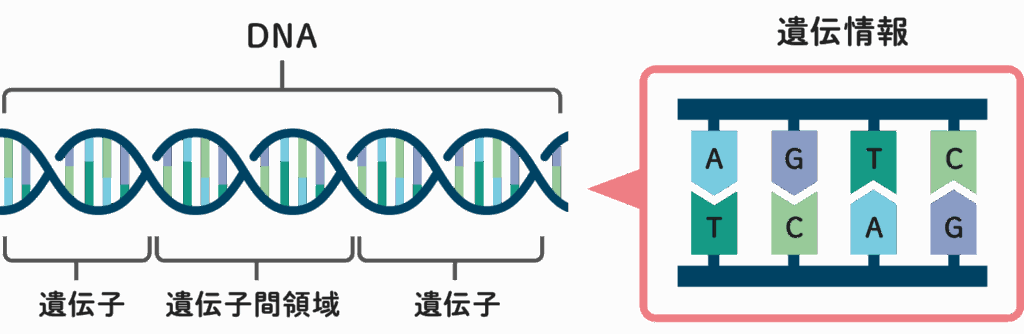
すべての遺伝情報の本体となるのが、DNA(デオキシリボ核酸)という化学物質です。DNAは、
- アデニン(A)
- チミン(T)
- グアニン(G)
- シトシン(C)
という4種類の文字(塩基)が長く連なってできており、この塩基の配列が遺伝情報を規定します。
②ゲノム
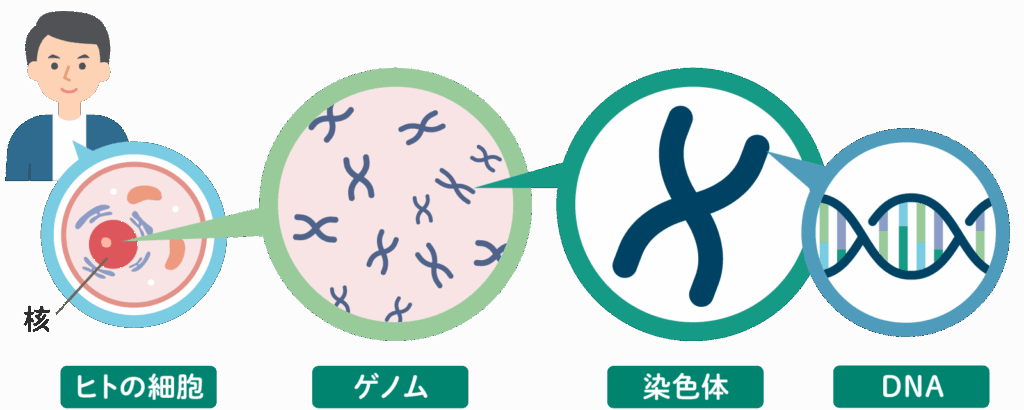
【ゲノムとは】
その生物が持つ遺伝情報の全体、つまりDNAのすべての配列情報をゲノムと呼びます。これは生命の「設計図の全巻セット」に例えられます。ヒトの場合、ゲノムは約32億もの塩基※の文字で構成されており、私たちの身体のすべてを形作るための膨大な情報がここに収められているのです。
③遺伝子
そして遺伝子とは、そのゲノムという設計図の中に記された、個別の具体的な機能を持つ部分を指します。例えば、特定のタンパク質を作るための情報などがそれに当たります。
「設計図の全巻セット」であるゲノムの中に、意味を持つ「章」や「節」として遺伝子が存在するイメージです。ヒトには約2万個の遺伝子があると考えられています。
ゲノム編集の基本原理
【ゲノム編集技術の原理】
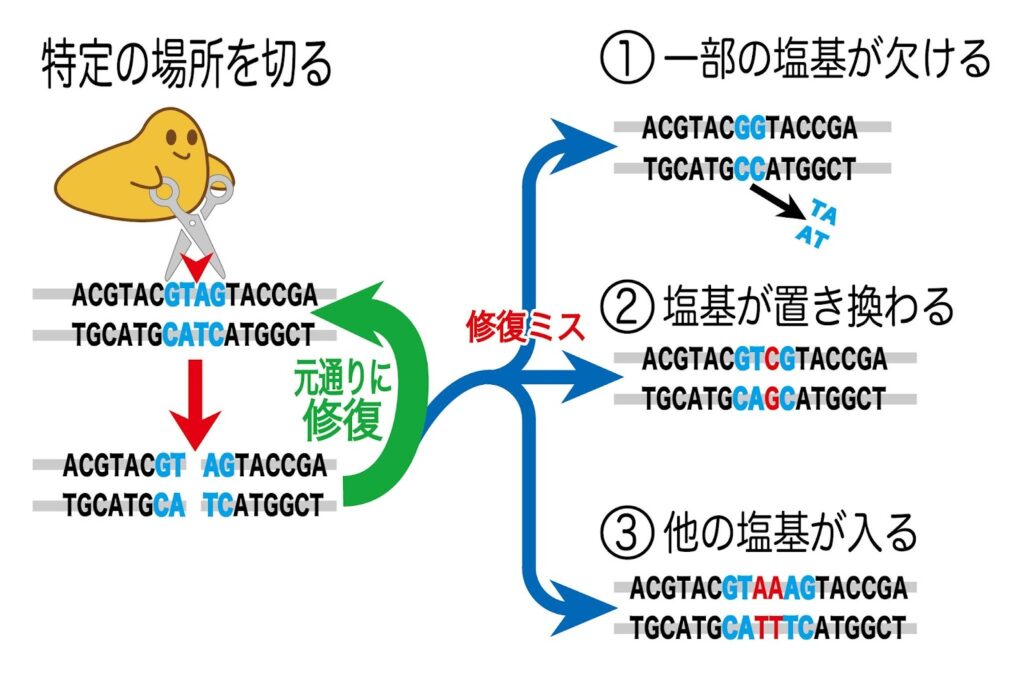
ゲノム編集の基本的な仕組みは、細胞がもともと持っている「切断」と「修復」という二つの自然な機能を巧みに利用することにあります。この技術では、まず人工的に作られた「分子のはさみ」の役割を持つ酵素を使い、ゲノム上の狙った場所のDNAを特異的に切断します。
DNAが切断された状態は、細胞にとって異常事態です。そのため、細胞はすぐに損傷を治そうと、備え付けの修復システムを働かせます。ゲノム編集は、この修復プロセスに介入することで、意図的に遺伝情報を書き換えるのです。
主な修復経路は二つあります。
非相同末端結合(NHEJ)
非相同末端結合(NHEJ)は、切断されたDNAの末端同士を直接つなぎ合わせる、迅速ですが間違いの起こりやすい修復方法です。この過程で数文字の欠落や挿入が起きることを利用し、特定の遺伝子を働かなくさせる「遺伝子ノックアウト」が実現できます。
相同組換え(HR)
相同組換え(HR)は、正常なDNA配列を設計図(鋳型)にして、切断箇所を正確に修復する仕組みです。このとき、お手本となる鋳型DNAを外から人為的に与えることで、狙った遺伝子を挿入したり、別の配列に置き換えたりする「遺伝子ノックイン」が可能になります。
この原理は、自然界で起こる突然変異を、特定の場所で意図的に、かつ高い確率で引き起こすものと考えることもできます。
ゲノム編集と遺伝子編集の違い
「ゲノム編集」と「遺伝子編集」は、しばしば同じ意味の言葉として使われますが、厳密には対象とする範囲にわずかな違いが見られます。
- 遺伝子編集:主にタンパク質の設計図である遺伝子部分の改変を指す
- ゲノム編集:遺伝子以外の領域(遺伝子の働きを調節する部分など)も含む、より広範なゲノム全体を対象
ただし、実際の技術はゲノム上のどの場所も狙うことができるため、現在ではより包括的な「ゲノム編集」という用語が一般的に使われる傾向にあります。重要なのは、どちらの言葉も「生命の設計図を、意図した通りに精密に書き換える技術」という点で共通していることです。
つまり、「遺伝子編集」は広義の概念であり、その中により精密で効率的な手法としての「ゲノム編集」が位置づけられると整理できます。また、ゲノム編集は「遺伝子を挿入する」のではなく、「既存の配列を削除・修復・書き換える」点が特徴であり、外来遺伝子を持たないケースが多いことも、社会的な受容性に関わる要素となっています。*1)
遺伝子組み換えとの違い

ゲノム編集の登場によって、生命科学の研究や農業技術が大きく進展しましたが、それ以前から注目されていた技術として「遺伝子組み換え」があります。どちらも「DNAを操作する技術」ですが、その手法や影響の大きさには明確な違いがあります。
遺伝子組み換えとは何か、さらにゲノム編集との違いを整理しておきましょう。
遺伝子組み換えとは
【遺伝子組換えによる育種】
出典:農林水産省『遺伝子組換えとは』p.6
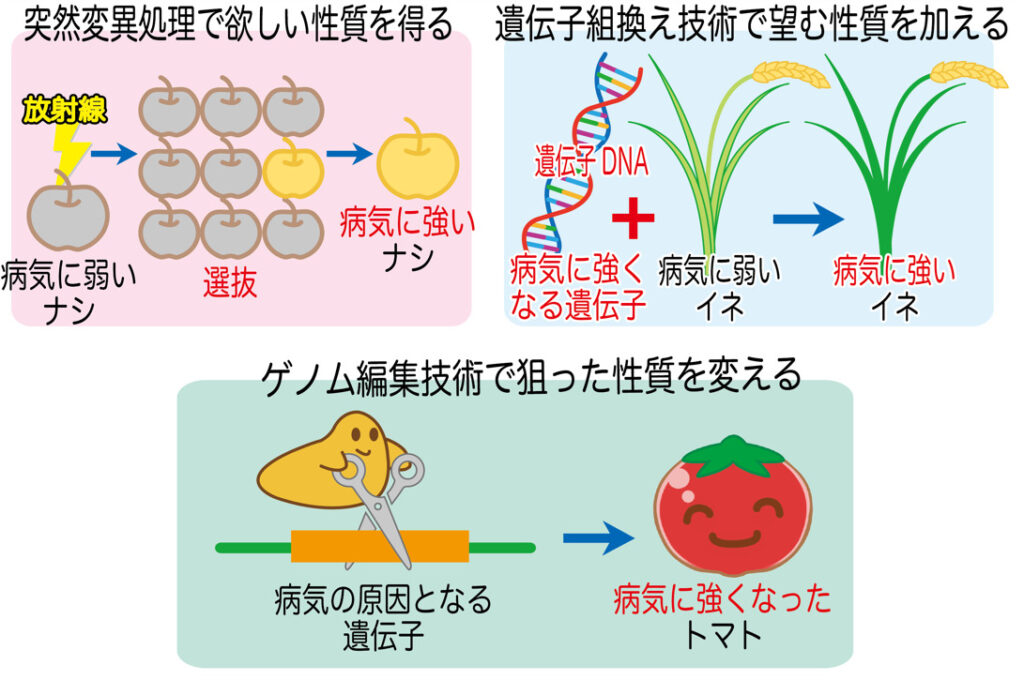
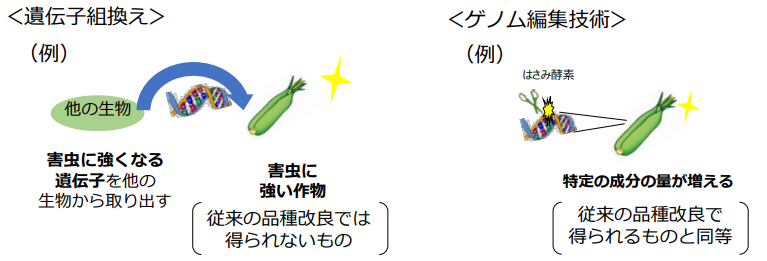
遺伝子組み換えとは、他の生物種から特定の遺伝子を取り出し、目的の生物に人工的に導入する技術です。1970年代に確立され、農作物や医薬品の分野で広く利用されています。
例を挙げると、殺虫性をもつ「Bt毒素遺伝子」をトウモロコシに導入することで、害虫に強い品種が生まれました。これは本来、まったく異なる種(この場合はバクテリア)の遺伝情報を用いている点が特徴です。
これにより耐性や成分の変化が起きるのですが、環境や生態系への影響が懸念され、規制や表示義務が国際的に課されています。
ゲノム編集との主な違い
【品種改良の方法は、どれも遺伝子の変化による性質の変化を利用】
ゲノム編集は、生物が本来もつ遺伝子の一部をピンポイントで「切って変える」手法です。外部の遺伝子を入れることなく、自らのDNAに小さな修正を加えるため、自然変異に近い結果を生み出せます。
この違いから、以下のように整理することができます。
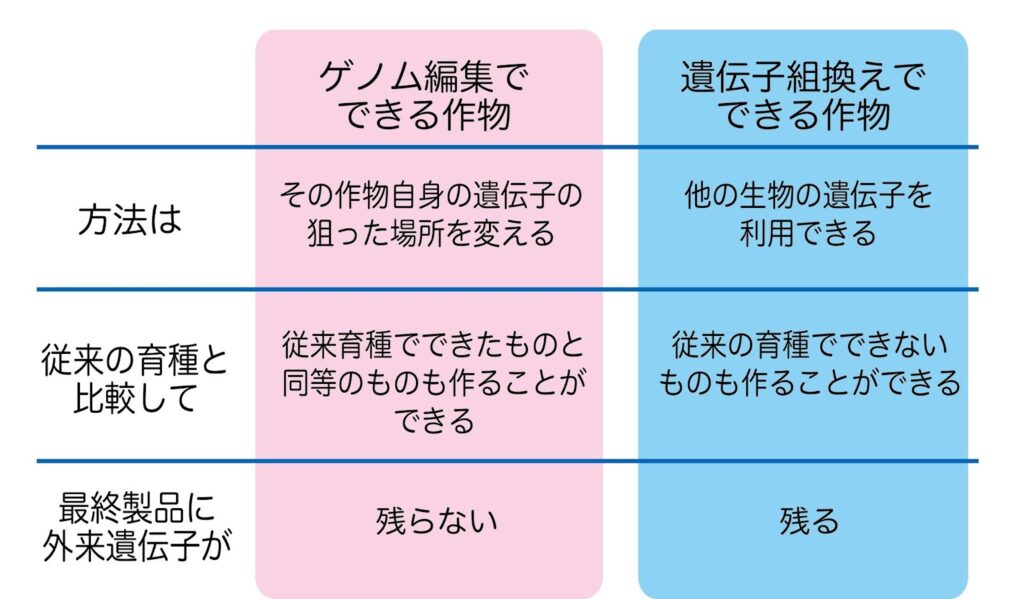
- 操作の精度:ゲノム編集は狙った場所だけを修正する。遺伝子組み換えは導入遺伝子が予期しない場所に組み込まれることがある。
- 外来遺伝子の有無:ゲノム編集では外部の遺伝子を使わずに改変が可能。遺伝子組み換えは原則として外部遺伝子を挿入する。
- 規制の違い:日本や米国では、外来遺伝子が残らないゲノム編集作物は遺伝子組み換えとみなされず、規制が緩いケースもある。(遺伝子組換え生物に該当せず、届出制で取り扱われる)
【ゲノム編集技術と遺伝子組換えの違い】
特に、2012年にCRISPR-Cas9という強力な編集技術を発表したジェニファー・ダウドナとエマニュエル・シャルパンティエの研究により、ゲノム編集は飛躍的に実用化が進みました。
【ゲノム編集と遺伝子組換え】
このように、
- 遺伝子組み換えは「他の生物由来の遺伝子を導入する技術」
- ゲノム編集は「自分の遺伝子を狙って書き換える技術」
と覚えておきましょう。
両者はともに生命を変える技術である一方で、そのアプローチと社会的な受容性は大きく異なります。次の章では、ゲノム編集が具体的にどのように行われているか、その方法を見ていきましょう。*2)
ゲノム編集の方法
【ゲノム編集による穂発芽耐性コムギ】
生命の設計図であるゲノムは、ヒトの場合30億文字にも及ぶ膨大な情報です。その中から特定の遺伝子だけを正確に見つけ出し、編集する。この「分子レベルの精密工学」とも呼べる作業は、一体どのように行われているのでしょうか。
ゲノム編集のプロセス
ゲノム編集のプロセスは、用いる技術が異なっても、基本的には三つの段階を踏みます。
- 探す:まず、ゲノムの中から編集したいDNA配列を正確に見つけ出します。
- 切る:次に、「分子のはさみ」となる酵素で、目的の場所のDNAの二本鎖を意図的に切断(Double-Strand Break, DSB)します。
- つなぐ:最後に、細胞がもともと持つ修復機能が働き、切断箇所を再結合します。このとき、修復ミスを利用して遺伝子を働かなくさせたり(NHEJ修復)、お手本となるDNA断片を加えて新たな配列を組み込んだり(HDR修復)するのです。
ゲノム編集のテクノロジー
この「分子のはさみ」は、世代ごとに進化を遂げてきました。第一世代のZFNや第二世代のTALENは画期的な技術でしたが、標的ごとに複雑なタンパク質を設計する必要がありました。
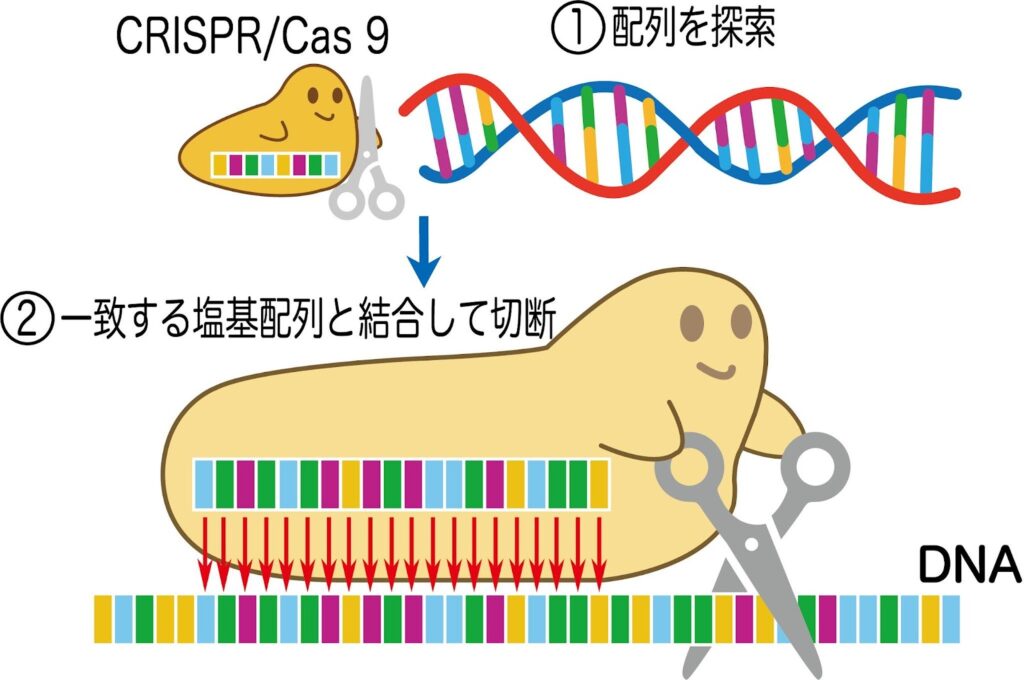
その常識を覆したのが、第三世代の革命的技術「CRISPR-Cas9(クリスパー・キャスナイン)」です。この技術は、二つのパーツが見事に連携して機能します。
- ガイドRNA(gRNA):「案内役」で、編集したい場所の配列情報を持つこの分子が、相方をゲノム上の正しい位置へとナビゲートします。
- Cas9(キャスナイン):「分子のはさみ」本体の酵素で、ガイドRNAに案内された場所で、DNAを正確に切断します。
【DNAを切断する「分子のはさみ(はさみ酵素)」】
このシステムの最大の革新は、案内役のガイドRNAの配列を変えるだけで、ゲノム上のあらゆる場所を狙える特徴にあります。この発見により、ゲノム編集は飛躍的に効率化し、世界中の研究室で利用されるようになりました。
さらに進んだ「切らないゲノム編集」とは
【4種類の塩基(A:アデニン、T:チミン、G:グアニン、C:シトシン)】
さらに技術は進歩し、より安全性を高めた「切らないゲノム編集」も登場しています。この代表的な技術である塩基編集(ベース・エディティング)※は、DNAを切断せず、4種類の塩基(A, T, G, C)のうちの1文字だけを、まるで鉛筆で書き換えるように直接修正する技術です。
これにより、遺伝病の原因となるたった一文字の間違いを、より安全に治療できる可能性が期待されています。
このようにゲノム編集技術は、驚くべき速度で進化を続けています。生命のプログラムを書き換える手法がより身近になったことは、社会にどのようなインパクトを与えているのでしょうか。次の章では、ゲノム編集が今、なぜこれほどまでに注目を集めているのか、その理由を掘り下げます。*3)
なぜゲノム編集は注目されているのか
【ゲノム編集によって作られた無花粉スギ】
驚くほどのスピードで進化を続けるゲノム編集技術が注目される理由は、単なる技術的な新しさだけにとどまりません。
- 技術の普及しやすさ
- 社会課題解決への期待
- 驚異的な市場の成長性
という三つの要素が相互に作用し、人類の未来を左右するゲームチェンジャーとして、世界中から熱い視線が注がれているのです。
①研究を加速させる革命的なシンプルさ
ゲノム編集が注目される根源的な理由は、CRISPR-Cas9の登場による技術の革命的な「シンプルさ」にあります。従来の技術では、標的ごとに複雑なタンパク質を設計する必要があり、多大な時間とコスト、高度な専門知識が必要でした。
しかしCRISPR-Cas9は、案内役のRNAを変えるだけで済むため、これらのハードルを劇的に下げたのです。
この革命は、ゲノム編集を一部の専門家の特別なツールから、世界中のあらゆる研究者が日常的に使える汎用技術へと変貌させました。結果として生命科学全体の研究開発スピードが飛躍的に向上し、これまで解明が難しかった生命現象や病気の原因究明が大きく進展しています。
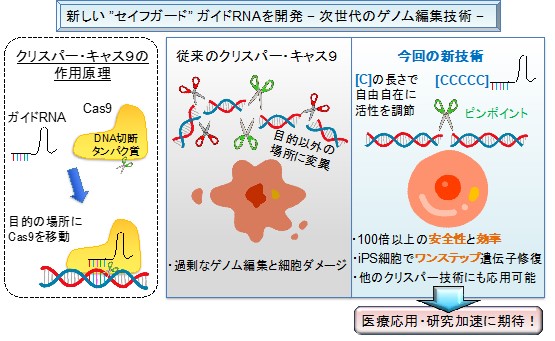
【新技術「セイフガードgRNA」】
さらに、2023年4月に発表された九州大学などが開発した新しいガイドRNA(セイフガードgRNA)は、RNAの末端に特定の塩基配列(シトシン)を付加することでCas9酵素の活性を精密に調整できます。過剰なゲノム切断を抑える「安全装置」として機能し、副作用のリスクを低減させながらゲノム編集の安全性と効率を飛躍的に高める次世代技術として期待されています。
②「不可能」を「可能」にする社会的インパクト
ゲノム編集は、私たちが直面する大きな課題に対する、強力な解決策となる可能性を秘めています。
その中でも最も期待が大きいのは医療分野です。これまで対症療法しかなかった多くの遺伝性疾患に対し、「原因となる遺伝子を直接修復する」という根本治療の道を開きました。これは医療の歴史における大きな転換点となり得ます。
また、食料・農業分野においても計り知れないインパクトを持ちます。従来の交配では数十年かかった品種改良を、わずか数年へと短縮可能です。
将来予測される世界的なタンパク質需要の増大に対し、
- 収穫量が多く栄養価の高い作物
- 病気に強く成長の速い魚
などを効率的に開発することは、持続可能な食料生産システムの鍵として期待されています。
③未来の成長を約束する巨大市場
ゲノム編集技術への期待は、その経済的なポテンシャルにも表れています。世界のゲノム編集市場は、年平均で20%を超える驚異的な成長率で拡大しており、2030年代初頭には数十兆円規模に達するとの予測も出ています。
この数字は、一般的な成長産業をはるかに凌ぐものであり、どれだけ多くの投資と期待がこの分野に集まっているかを物語っています。この市場の成長は、先述の医療や農業での実用化が現実のものとなってきていることの証しといえるでしょう。
このように、ゲノム編集は技術的な革新性を基盤に、社会的な課題解決への期待と巨大な経済的価値が一体となって、世界的な注目を集めています。では、この大きな期待が寄せられる技術は、私たちに具体的にどのようなメリットをもたらすのでしょうか。*4)
ゲノム編集のメリット

生命の設計図を自在に書き換えるゲノム編集は、私たちの社会にどのような恩恵をもたらすのでしょうか。そのメリットはすでに、最先端の研究現場から、未来の医療、そして日々の食卓にまで及んでいます。
生命科学の発展を加速させる研究ツール
ゲノム編集、特にCRISPR-Cas9の登場は、生命科学の研究スピードを劇的に向上させました。従来は専門家が数ヶ月~数年かけていた遺伝子解析や疾患モデル動物の作製が、今ではより多くの研究者によって短期間で行えます。
この「研究の効率化」は、
- 病気の原因解明
- 新薬開発
- 疾患モデル動物・細胞モデル作製
- 農作物・畜産品種改良
といった、さまざまな分野の発展を加速させる基盤となっています。
医療に「根本治療」という選択肢を
ゲノム編集は、これまで症状を抑えることしかできなかった病気に対し、「根本治療」という画期的な選択肢をもたらします。遺伝子の異常によって引き起こされる難病に対し、その設計図を直接修復するアプローチが現実のものとなりました。
また、患者自身の免疫細胞の力を高めてがんと戦わせるなど、これまでとは全く異なる発想の治療法開発も進んでおり、医療に革命を起こす力を持っています。
持続可能な食料生産への貢献
農業や水産業において、ゲノム編集は品種改良にかかる時間を数十年から数年へと大幅に短縮します。これにより、少ない肥料で育つ作物や、病気に強く成長の速い魚などを効率的に開発できます。
例えば、以下のような農水産物が作られています。
- 高栄養の農産物
- 省肥料高収量のイネ
- 耐塩性・耐乾性のイネ
- 可食部が多い魚
- 成長速度の早い魚
これらは食料の安定供給に貢献するだけでなく、環境負荷の少ない持続可能な農業・水産業の実現にも繋がる、大きなメリットといえるでしょう。
ゲノム編集は、
- 研究を加速
- 医療を刷新
- 食の未来を支える
という多大な恩恵をもたらします。しかし、この強力な技術には障壁もあります。次の章では、ゲノム編集が抱えるデメリットや課題について詳しく見ていきます。*5)
ゲノム編集のデメリット・課題

計り知れない恩恵をもたらす可能性を秘めたゲノム編集ですが、その強力さゆえに、技術的・倫理的に乗り越えるべき重要な課題も存在します。この技術を社会が賢明に利用していくためには、このような負の側面にも真摯に向き合う必要があります。
技術的な安全性:オフターゲットとモザイク現象
ゲノム編集の安全性における最大の課題は、意図しない遺伝子を編集する「オフターゲット」と、一部の細胞しか編集されない「モザイク現象」です。
オフターゲット
オフターゲットは、狙った場所以外で変異を引き起こすリスクを指します。過去には、マウス実験で多数の予測不能な変異が報告され、安全性が大きく懸念されました。
しかし、その後の複数の研究では、解析手法の改善によりオフターゲット頻度は当初の懸念より遥かに低いという報告もなされており、正確なリスク評価は今なお続いています。
モザイク現象
モザイク現象は、受精卵などを編集した際に、体内で編集された細胞と未編集の細胞が混在してしまう状態を指し、治療効果の低下や正確な評価を困難にします。この課題に対し、編集を行うタイミングを最適化するなど、モザイクの発生を低減させるための技術開発も進められています。
倫理と法整備:許される範囲と社会のルール
ゲノム編集の、特にヒトへの応用は深刻な倫理的ジレンマを持っています。個人の治療を目的とした体細胞の編集と異なり、精子や卵子、受精卵といった「生殖細胞系列」の編集は、その変更が子孫へ永続的に受け継がれるため、社会に重大な影響を及ぼしかねません。
日本では、文部科学省・厚生労働省の「ヒト受精胚に遺伝情報改変技術等を用いる研究に関する倫理指針」(2019年策定、その後改定)などに基づき、基礎研究は認められているものの、編集した受精卵をヒトや動物の胎内に戻すことは固く禁止されています。しかし、これらは罰則を伴う法律ではないため、規制の実効性には限界があるとの指摘もあります。
技術の急速な進歩に対し、社会的な合意形成と実効性のあるルール作りが追いついていないのが現状です。
このように、ゲノム編集は技術的な安全性の確立と、生命倫理という根源的な問いの両方に直面しています。これらの課題に社会全体で向き合い、適切なルールを構築していくことが、この技術の未来にとって不可欠といえるでしょう。*6)
ゲノム編集の活用事例
【上:ゲノム編集したトラフグ、下:通常のトラフグ】
ゲノム編集は「理論」から「実用」の時代へと突入し、その恩恵はすでに私たちの社会に届き始めています。医療現場では難病の根治が現実となり、食卓には新しい機能を持つ食品が並ぶなど、具体的な成果が次々と生まれています。
医療分野:世界初の治療薬承認と日本の挑戦
ゲノム編集医療は歴史的な転換点を迎えました。2023年12月、アメリカ食品医薬品局(FDA)は、遺伝性の血液疾患である鎌状赤血球症に対する世界初のゲノム編集治療薬「Casgevy」※を承認しました。
さらに2024年1月には、輸血に依存するβサラセミア※の治療薬としても米国で承認されています。臨床試験では、治療を受けた患者の93.5%が1年以上にわたり激しい痛みの発作(血管閉塞性発作)※を経験しないという高い効果を示しました。
治療価格は約3億2,000万円と高額ですが、従来の治療で生涯にかかる医療費が5億円を超えるともいわれる中、一度の治療で根治が期待できる経済的意義も注目されます。
また、日本ではデュシェンヌ型筋ジストロフィー※などに対する遺伝子治療法が実用化研究段階にあり、iPS細胞とゲノム編集を組み合わせた難病研究も活発に進められています。
農業・水産分野:食卓に届く新しい恵み
【シシリアンルージュハイギャバ(左)とのゲノム編集したマダイ(右)】
私たちの食に直結する分野でも、ゲノム編集技術は社会実装のフェーズに入っています。
日本では、
- 機能性成分「GABA」※を豊富に含むゲノム編集トマト「シシリアンルージュハイギャバ」
- 筋肉量を増やした「22世紀鯛」
- 成長速度を高めた「22世紀ふぐ」
などが開発されました。これらは、厚生労働省や農林水産省への届出が受理され、すでに市販されています。
一方で、作物の日持ちを良くする技術や新しい編集手法なども研究・開発されていますが、これらの革新的な研究は、現時点ではまだ実用化されていません。
ただ、2026年3月時点では本格的拡大には至らず、社会で気議論が進行中です。
このような事例は、ゲノム編集がもはや夢物語ではなく、現代社会の課題を解決する現実的なツールであることを強く示しています。しかし、その開発の道のりは常に順風満帆なわけではありません。次の章では、ゲノム編集技術が直面した失敗事例について見ていきます。*7)
ゲノム編集の失敗事例

大きな可能性を秘めたゲノム編集ですが、その輝かしい成果の裏には、技術的な問題や倫理的な過ちによって引き起こされた「失敗」も存在します。これらの事例は、この技術の健全な発展のために私たちが学ぶべき、重要な教訓となっています。
倫理を揺るがしたヒト受精卵の編集事件
2018年、中国の研究者がHIVへの耐性を持たせる目的で、世界で初めてゲノム編集ベビーを誕生させました。この失敗は技術面ではなく、子孫に受け継がれるヒト受精卵の改変という、国際的に禁じられた倫理の壁を、十分な検証や社会的な議論なく秘密裏に破った点にあります。
将来世代への未知のリスクを無視したこの行為は、世界中の科学界から厳しく非難されました。
予期せぬ遺伝子が混入した「角なし牛」
農業分野では、技術的な盲点が浮き彫りになった事例があります。アメリカで、痛みを伴う除角作業を不要にする角なし牛がゲノム編集で開発されました。
しかし後のFDAの解析で、編集過程で使われた抗生物質耐性遺伝子を含む異種のDNA断片が、意図せずゲノムに組み込まれていたことが発覚しました。狙い通りの改変でも、想定外の遺伝子変化が起こりうるリスクと、厳密な検証体制の重要性を示しました。
遺伝子ドライブ蚊に生まれた「耐性」
生態系そのものを改変する試みも、自然が持つ進化の力の強さに直面しています。マラリアを媒介する蚊を根絶するため、メスを不妊にする遺伝子を特定の集団に強制的に広める「遺伝子ドライブ」が開発されました。しかし世代を重ねる中で、編集を回避できる「耐性」を持つ蚊が自然に出現したのです。
この耐性を持つ個体が選択的に増え、最終的に駆除効果は失われました。生態系に介入する技術が、進化の力で無力化されうる困難さを示す事例です。
これらの失敗は、ゲノム編集という強力なツールを扱う上での、科学者の責任と社会的なルールの必要性を浮き彫りにします。技術の可能性を活かしつつ、負の側面をいかにコントロールしていくかが、今後の大きな課題です。*8)
ゲノム編集とSDGs
【2020年ノーベル化学賞を受賞したシャルパンティエ所長(左)ダウドナ教授(右)】
ゲノム編集技術とSDGs(持続可能な開発目標)は、科学技術を用いて地球上の生命が直面する課題を解決し、より豊かで持続可能な未来を築くという点で、その理念を共有しています。生命の設計図に直接働きかけるこの革新的な技術は、特に
- 食料
- 健康
- 環境
の分野で、従来の延長線上では達成が困難だった目標への道を拓く可能性を秘めています。
SDGs目標2:飢餓をゼロに
ゲノム編集は、気候変動下での食料安全保障の確立に大きな期待が寄せられる技術です。従来の品種改良を大幅に上回るスピードで、病気や環境の変化に強く、少ない肥料でも育つ作物や、栄養価を高めたトマト、短期間で効率的に成長する魚などの開発がすでに実現しています。
これにより、食料の安定供給と品質向上が可能になり、飢餓の撲滅に直接的に貢献します。
SDGs目標3:すべての人に健康と福祉を
この技術は、すべての人々の健康と福祉にも大きく寄与します。これまで根本治療が難しかった遺伝性疾患に対し、ゲノム編集は病気の原因そのものを修復する医療を可能にしました。
世界で初めて承認されたゲノム編集治療薬「Casgevy(exagamglogene autotemcel)」も登場し、一度の処置で生涯のQOL(生活の質)を劇的に改善する道を開いています。これは医療へのアクセスや経済状況による健康格差の是正にも繋がる可能性を秘めています。
SDGs目標9:産業と技術革新の基盤をつくろう
ゲノム編集は、新たな産業を生み出す技術革新の重要な鍵です。画期的な治療薬や高機能食品などの開発は、急成長するバイオ関連市場を牽引し、持続可能な産業の構築と質の高い雇用の創出に貢献します。
この分野への活発な投資と研究開発は、未来の産業基盤そのものを強靭なものにします。
SDGs目標14:海の豊かさを守ろう
ゲノム編集は、海の生態系保全と持続可能な水産業の実現にも貢献します。病気に強く、より少ない餌で早く育つ魚を開発することで、養殖による環境負荷や天然資源への依存を減らすことが可能です。
将来的には、海水温の上昇に耐性を持つサンゴを開発するなど、気候変動から海の豊かさを守る研究も模索されています。
このようにゲノム編集は、健康や食料から産業、環境保全まで、SDGsの多様な目標達成に貢献する横断的な基盤技術です。その責任ある活用によって、持続可能な社会への移行を加速させる強力な推進力となります。*9)
>>SDGsに関する詳しい記事はこちらから
まとめ
ゲノム編集(遺伝子編集)とは、生物が持つ遺伝情報の全体(ゲノム)の中から、特定の遺伝子を狙ってその働きを変えたり、別のものに置き換えたりする技術です。「分子のはさみ」と呼ばれる酵素などを用いてDNAの配列を精密に書き換えることで、病気の治療や農作物の品種改良など、幅広い分野での応用が期待されています。
近年では、先進国では遺伝性疾患の治療薬が次々と実用化され、また一方では開発途上国などの地域の食料安全保障に貢献する作物の研究が進むなど、その応用は世界中に広がっています。しかし、ゲノム編集は、医療や食料問題に革命をもたらすと同時に、倫理や安全面で重い課題を抱える技術です。
この大きな可能性と課題を秘めた技術を、人類全体の幸福に繋げるためには、まだ多くの対話や議論が必要です。先進国で開発される高価な医療と、途上国で求められる食料増産との間に、技術や恩恵の格差が生まれてはいけません。
国や文化、経済状況の違いを超えて、技術の恩恵を誰もが公正に享受できる国際的なルール作りと、生命に対する深い倫理観の共有が、今まさに求められています。
この技術が創る未来の、私たちは当事者です。ゲノム編集の光と影の両面を正しく知り、自分自身の問題として考えることが、より良い未来を選択する第一歩となります。
私たちは、生命の設計図をどこまで書き換えることを許容すべきでしょうか。
この答えを出すのは簡単ではないかもしれません。それでも、この計り知れない可能性を持つ技術に常に関心を持ち、学び、考え続けることが、より良い未来の実現に向けた、私たち一人ひとりにできる確かなアクションです。*10)
<参考・引用文献>
*1)ゲノム編集・遺伝子編集とは
がんゲノム情報管理センター『よく分かるがんゲノム医療とC-CAT』
農林水産技術会議『ゲノム編集~新しい育種技術~』
名城大学『What’s ゲノム編集?』
産業技術総合研究所『ゲノム編集とは?―遺伝子組換えとの違い―科学の目でみる、 社会が注目する本当の理由』(2022年8月)
研究開発戦略センター『ゲノム編集技術』(2014年)
研究開発戦略センター『2.3.7 ゲノム編集・エピゲノム編集』(2023年2月)
ALFS『ゲノム・遺伝子・DNAの違いをわかり易く解説!それぞれの特徴は?』(2024年12月)
理化学研究所『DNAからの遺伝情報を伝達するメカニズムを解明- X線結晶構造解析により明らかになったRNAポリメラーゼの反応機構 -(プレスリリース)』(2002年10月)
東京工業大学『数多の産業の未来を切り開くゲノム編集技術』
Wikipedia『ゲノム編集』
Wikipedia『エマニュエル・シャルパンティエ』
Thermo Fisher Scientific『ゲノム編集の原理と手引き~CRISPR/Cas9とは?』(2023年7月)
NTT『ゲノム編集とは?遺伝子組換えとの違いや危険性、応用の可能性を解説』(2023年9月)
ビジネス+IT『ゲノム編集とは何か? 従来の遺伝子治療と何が違う?具体的な実用事例からみる可能性』(2018年8月)
*2)遺伝子組み換えとの違い
農林水産省『遺伝子組換えとは』
農林水産技術会議『ゲノム編集~新しい育種技術~』
農林水産省『ゲノム編集技術を利用した品種改良と得られた農林水産物の取扱い』(2025年5月)
消費者庁『遺伝子組換え食品』(2023年3月)
神奈川県衛生研究所『『ゲノム編集食品』ってなに?『遺伝子組換え食品』とはどう違うの?』(2023年9月)
日本育種学会『ゲノム編集生物のカルタヘナ法下における取り扱い方針について』
在日フランス大使館『2020年ノーベル化学賞にフランス人研究者エマニュエル・シャルパンティエ氏』(2021年6月SciencePortal『今年のノーベル賞【後編】化学賞の欧米女性2氏 プエルトリコで運命的な出会い、共同研究へ』(2020年10月)
農林水産省『ゲノム編集~新しい育種技術~』
農林水産省『生物多様性と遺伝子組換え(基礎情報)』
農林水産省『遺伝子組換えパパイヤに関する情報(詳細)』
農林水産省『遺伝子組換え(いでんしくみかえ)技術について教えてください。』
田部井 豊『ゲノム編集食品の規制と国際動向』(2019年)
環境省『ゲノム編集技術の概念の整理につい』(2018年7月)
環境省『カルタヘナ法におけるゲノム編集技術の利用により得られた生物の規制対象範囲(案)』(2018年)
Bio-Station『国内での取扱いルール』
農研機構『QVII- 1 遺伝子組換え食品の表示制度に関する法律について教えてください。』
厚生労働省『ゲノム編集技術を利用して得られた食品等に関する意見交換会』
国立医薬品食品衛生研究所『遺伝子組換え食品・ゲノム編集食品 Q&A』
*3)ゲノム編集の方法
農林水産技術会議『ゲノム編集~新しい育種技術~』
日本医学会連合『5.2新たなゲノム編集技術開発の現状』
COSMO BIO『特集:CRISPR-Cas9 とは』
神戸大学『最高精度かつ最小サイズの塩基編集技術の実現』(2022年8月)
長船 健二『ゲノム編集と iPS 細胞』(2018年)
東京都医学総合研究所『CRISPR/Cas9によるDNA組換えを介した正確なゲノム編集を促進する条件を発見』(2019年1月)
VectorBuilder『CRISPRとTALENどちらをゲノム編集に使うべき?』
Thermo Fisher Scientific『ゲノム編集の原理と手引き~CRISPR/Cas9とは?』(2023年7月)
Bio-Station『最新バイオテクノロジーを使った品種改良-ゲノム編集技術を用いた品種改良-』
Bio-Station『もう偶然には頼らない!目的箇所を希望の配列に書き換える精密ゲノム編集技術』(2020年7月)
河合 康洋『ゲノム編集技術の現状と可能性』(2016年)
日本生化学会『CRISPR-Cas9の構造と機能』(2015年12月)
乾 雅史『ゲノム編集の現状について』
東邦大学『CRISPR/Cas9を用いたゲノム編集』
木下 政人『次世代の遺伝子改変技術としてのゲノム編集 基本原理を中心に』(2015年)
農研機構『植物ゲノム編集ツールの拡充―改良型 Cas9 を用いた植物ゲノム編集―』(2019年4月)
研究開発戦略センター『2.3.7 ゲノム編集・エピゲノム編集』(2023年2月)
*4)なぜゲノム編集は注目されているのか
農林水産技術会議『ゲノム編集~新しい育種技術~』
九州大学『ゲノム編集の効率や安全性を100倍以上高める新技術を開発 遺伝子治療の実用化を加速する次世代型ゲノム編集法として期待』(2023年4月)
経済産業省『バイオものづくり革命の実現』(2023年4月)
NEDO『バイオものづくり革命推進事業』
厚生労働省『ゲノム編集技術の臨床応用について』(2017年4月)
研究開発戦略センター『第73回「CRISPR/Cas9 ゲノム編集 技術革新」』(2020年10月)
PEAKS MEDIA『CRISPR-Cas9とは?原理や特徴・倫理的な問題についてわかりやすく解説』(2024年10月)
Research Nester『ゲノム編集市場調査、規模、傾向のハイライト(予測2024-2036年)』(2023年10月)
H&I Global Research『世界のゲノム編集市場(2025年~2030年):技術別(CRISPR/Cas9)、投与方法別(エクソビボ)、用途別(遺伝子工学、臨床応用)、提供形態別(契約、自社開発)、最終用途別、地域別』(2025年4月)
Global Information『ゲノム編集市場の市場規模、シェア、動向分析レポート:技術別、送達方法別、用途別、モード別、最終用途別、地域別、セグメント予測、2025年~2030年』(2025年4月)
日本政策投資銀行『我が国におけるバイオものづくりの産業化に向けて』(2023年3月)
横浜市立大学『世界初 スギのゲノム編集技術を開発 ~針葉樹の品種改良を⼤幅に短縮する新技術として期待~』(2021年9月)
生物系特定産業技術研究支援センター『精密ゲノム編集技術による品種改良の効率化』
日本医学連合会『3.2 遺伝子治療法、ex vivoゲノム編集治療、in vivoゲノム編集治療とは』
首相官邸『遺伝子治療とゲノム編集治療の研究開発の現状と課題』
内閣府『バイオエコノミー戦略』(2024年6月)
名古屋大学『ゲノム編集の効率や安全性を 100 倍以上高める新技術を開発 遺伝子治療の実用化を加速する次世代型ゲノム編集法として期待』(2023年4月)
九州大学『ゲノム編集の効率や安全性を 100 倍以上高める新技術を開発 遺伝子治療の実用化を加速する次世代型ゲノム編集法として期待』(2023年4月)
京都大学『高効率で自在なゲノム改変技術の開発に成功』(2018年2月)
東洋経済ONLINE『「ゲノム編集食品」で食料自給率は上がるか テクノロジーを活用した新しい農業の未来』(2022年9月)
石野 良純『CRISPR/Cas9を利用したゲノム編集の原理とアレルギー疾患への応用』(2023年)
西分 千秋『ゲノム編集食品が食卓へー表示とトレーサビリティの必要性ー』(2020年10月)
Nipponham『プロテインクライシスの真実と、たんぱく質の安定供給への取り組み① 日本から「肉」がなくなるって本当?』
*5)ゲノム編集のメリット
九州大学『ゲノム編集の効率や安全性を100倍以上高める新技術を開発遺伝子治療の実用化を加速する次世代型ゲノム編集法として期待』(2023年4月
理化学研究所『ゲノム編集による高効率ノックインマウスの作製-細胞周期が作製効率の鍵を握る-』(2020年6月)
日本医学連合会『3.3ゲノム編集の医学応用の具体例』
日本医学連合会『2.3ゲノム編集の応用例(治療応用を除く)』
農研機構『(研究成果) 外来DNAをもたないゲノム編集植物の作出を大幅に効率化- ゲノム編集の適用作物拡大に期待 -』(2025年7月)
大阪大学『新規ゲノム編集技術を用いた難治性遺伝病に対する根治療法の開発 (Development of curative therapies for intractable genetic diseases using novel genome editing technologies)』(2023年3月)
笹川平和財団『ゲノム編集による養殖魚育種の加速化』(2022年5月)
農林水産技術会議『養殖魚品種改良期間の劇的な短縮を実現する革新的早期精子形成技術の開発』(2017年)
VectorBuilder『CRISPRの最適化:効率の良い遺伝子編集のための技術とアプローチ』(2025年3月)
日本医療研究開発機構『遺伝子編集でさまざまな疾患への創薬に応用可能な技術を確立』(2019年)
日本医療研究開発機構『筋ジストロフィーのゲノム編集治療を目指したLNP-mRNA輸送システムの開発』(2022年1月)
三浦 浩美『in vivoゲノム編集効率の最適化と疾患モデル動物遺伝子治療への応用』(2020年3月)
産業技術総合研究所『日本発のゲノム編集ツールで新たな道を開く!』(2024年5月)
神戸大学『エイズウイルスの調節遺伝子を標的とするゲノム編集法でウイルス遺伝子を不活化』(2018年5月)
京都大学『筋ジストロフィーのゲノム編集治療を目指したLNP-mRNA輸送システムの開発』(2021年12月)
髙田 和秀『HIV 垂直感染予防を目的としたゲノム編集児誕生の是非』(2019年)
水産総合研究センター『水産ゲノム研究戦略』(2010年3月)
*6)ゲノム編集のデメリット・課題
京都大学『チンパンジー親子トリオ(父親-母親-息子)の全ゲノム配列を高精度で解明』(2017年11月)
遠藤 亮,賀屋 秀隆,土岐 精一『CRISPR/Cas9によるゲノム編集技術の進展と作物への応用
発展し続けるCRISPR/Cas9を用いたゲノム編集技術』(2018年)
田中 光一『ゲノム編集』(2019年5月)
理化学研究所『ゲノム編集による高効率ノックインマウスの作製-細胞周期が作製効率の鍵を握る-』(2020年6月)
京都大学『ゲノム編集技術を用いてカニクイザルモデルにおいて常染色体優性多発性嚢胞腎(ADPKD)の病態再現に成功』(2019年12月)
東京大学『ヒト受精胚ゲノム編集』
日本人類遺伝学会『「ヒト受精胚に遺伝情報改変技術等を用いる研究に関する倫理指針」及び「ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針」の一部改正について周知依頼が届きました。』(2021年8月)
厚生労働省『ヒト受精胚に遺伝情報改変技術等を用いる研究に関する倫理指針ガイダンス』(2023年3月)
日本経済新聞『ゲノム編集ベビー、誕生させた中国の研究者に懲役3年』(2019年12月)
Yahoo!ニュース『ゲノム編集ベビーの賀建奎博士に懲役3年の実刑判決 では、日本で起きたら?』(2019年12月)
日本学術会議『ゲノム編集技術のヒト胚等への臨床応用に対する法規制のあり方について』(2020年3月)
河合 康洋『ゲノム編集技術の現状と可能性』(2016年)
大野 聖子『遺伝子診断・ゲノム解析の最前線』(2023年)
Springer Nature『ヒト胚ゲノム編集の波紋』
厚生労働省『諸外国におけるゲノム編集技術等を用いたヒト胚の取扱いに係わる法制度や最新の動向調査及びあるべき日本の公的規制についての研究』(2020年9月)
SCIENCE TOKYO『標的認識の特異性が高い、日本独自のゲノム編集技術』(2023年3月)
*7)ゲノム編集の活用事例
農林水産技術会議『ゲノム編集~新しい育種技術~』
経済産業省『バイオテクノロジーが拓く『第五次産業革命』』(2021年2月)
FDA『FDA Approves First Gene Therapies to Treat Patients with Sickle Cell Disease』(2023年12月)
FDA『CASGEVY』
PMC『Editorial: First Regulatory Approvals for CRISPR-Cas9 Therapeutic Gene Editing for Sickle Cell Disease and Transfusion-Dependent β-Thalassemia』(2024年3月)
PMC『FDA approval of Casgevy and Lyfgenia: a dual breakthrough in gene therapies for sickle cell disease』(2024年7月)
MJH Life Sciences『FDA Accepts Exa-cel BLA for Sickle Cell and Transfusion-Dependent β-Thalassemia』(2023年6月)
American Society of Hematology『Full Results of Exa-Cel Study Show Continued Safety, Efficacy in Sickle Cell Disease』(2024年8月)
CRISPR『CRISPR Therapeutics Announces U.S. Food and Drug Administration (FDA) Approval of CASGEVY™ (exagamglogene autotemcel) for the Treatment of Transfusion-Dependent Beta Thalassemia』(2024年1月)
筑波大学『「食と先端技術共創コンソーシアム」シシリアンルージュハイギャバについて食品新聞に掲載』(2023年8月)
京都大学『京大発、「肉厚マダイ」参上 食に革命を起こすゲノム編集と安全』(2018年6月)
日本経済新聞『「GABA」5~6倍のトマト苗配布 筑波大発新興ゲノム編集技術で開発、5月から』(2021年4月)
日経BP『320万円集めた「ゲノム編集マダイ」とは? 仕掛け人が語る野望』(2021年10月)
日経BP『トラフグの成長速度約2倍、ゲノム編集で漁業を成長産業に』(2022年2月)
VERTEX『Vertex Announces US FDA Approval of CASGEVY™ (exagamglogene autotemcel) for the Treatment of Transfusion-Dependent Beta Thalassemia』(2024年6月)
VERTEX『How CASGEVY® Is Being Studied』
Goodwin『FDA Approves First Cell-Based Therapies for Treatment of Sickle Cell Disease』(2023年12月)
関とら『ふく百話(28)「22世紀ふぐ」』
ふぐマガ『トラフグ養殖技術に新たな一歩? ゲノム編集トラフグについて』(2021年11月)
*8)ゲノム編集の失敗事例
American Association for the Advancement of Science『CRISPR bombshell: Chinese researcher claims to have created gene-edited twins』(2018年11月)
BBC『China jails ‘gene-edited babies’ scientist for three years』(2019年12月)
Biosafety Information Centre『Genome-Edited Hornless Cattle Found to Have Unintended Antibiotic Resistance Genes』(2019年9月)
Agricultural Research Service『Scientists Use Gene-Editing Technology to Produce First Calf Resistant to Major Viral Disease』(2023年5月)
FDA『FDA Clarifies Approach to Genomic Alterations in Animals』(2024年5月)
ISAAA『Genome-Edited Cattle Soon to Hit the US Market after FDA Rules it Low-Risk』(2022年3月)
AVMA『Genetically modified cattle may be sold for food in U.S.』(2022年3月)
TESTBIOTECH『Genetically engineered hornless cattle: flaws in the genome overlooked』(2019年8月)
nature『遺伝子ドライブでマラリアと闘う』
日立財団『遺伝子ドライブの倫理的・法的・社会的課題に関する環境衛生倫理学的考察』(2023年3月)
京都大学『全米科学・工学・医学アカデミー『近未来の遺伝子ドライブ』概要』
BBC『遺伝子組み換え菌、マラリア媒介の蚊を強力駆除=最新研究』(2019年5月)
日本経済新聞『遺伝子組み換え蚊、感染対策の切り札に 米国で実証試験』(2023年5月)
*9)ゲノム編集とSDGs
農林水産省『ゲノム編集技術の社会実装と農林水産業の未来像』(2020年12月)
科学技術振興機構『養殖技術で「海を耕す!」─近畿大学水産研究所』(2020年9月)
生物系特定産業技術研究支援センター『《こぼれ話10》ゲノム編集で健康によいトマトが誕生』(2020年8月)
日本経済新聞『気候変動に強いイネ、野生種を高速改良へ 国立遺伝研』(2023年7月)
岡山大学『第76回岡大SDGsサイエンスカフェ『「ゲノム編集」作物が開く未来の可能性』『遺伝子パネル検査とは? -がんゲノム医療最前線-』【オンライン開催】』(2020年9月)
日本学術会議『SDGsから見た学術会議 ―社会と学術の関係を構築する―』
大阪公立大学『ゲノム編集技術で ユーグレナが作り出す油脂のコントロールに成功!』(2024年9月)
東京工業大学『油糧藻類における遺伝子改変後に脱落可能なゲノム編集ベクターの開発』(2022年3月)
広島大学『ゲノム編集によるバイオ産業創出』
全日本科学技術協会『バイオDXによるデータ駆動型ゲノム育種=デジタル育種』(2021年4月)
日本水産学会『水産育種研究会「変革的技術融合による養殖業の強靭化にかかる国際会議」(2024年10月28日~30日開催)』(2024年7月)
理化学研究所『ゲノム編集で遊泳不全ミドリムシの作出に成功』(2022年9月)
東京農業大学『植物の“水欠乏・高温耐性”を強化する遺伝子の単離・解析』
中央大学『CRISPR/Cas9を用いた単細胞性緑藻コッコミクサのゲノム編集に成功~ 産業用微細藻のゲノム編集が本格化へ ~』(2018年12月)
建石 真公子『日本における研究目的の「ヒト胚のゲノム編集」と「ヒト胚の作成」─人権の観点からどう考えるか』(2020年10月)
農研機構『植物ゲノム編集の効率化』
日本学術学会『人の生殖にゲノム編集技術を用いることの倫理的正当性について』(2020年)
境 新一『SDGs と農作物の品種改良・新技術の展開に関する考察』(2019年12月)
岡山大学『遺伝子改変技術でストレスに強いオオムギを作り出す』
ユーグレナ『微細藻類ユーグレナのゲノム編集技術を拡張-より柔軟かつ緻密なゲノム改変が可能に-』(2024年2月)
*10)まとめ
『ゲノム編集技術を利用した品種改良と得られた農林水産物の取扱い』(2025年5月)
この記事を書いた人
松本 淳和 ライター
生物多様性、生物の循環、人々の暮らしを守りたい生物学研究室所属の博物館職員。正しい選択のための確実な情報を提供します。趣味は植物の栽培と生き物の飼育。無駄のない快適な生活を追求。
生物多様性、生物の循環、人々の暮らしを守りたい生物学研究室所属の博物館職員。正しい選択のための確実な情報を提供します。趣味は植物の栽培と生き物の飼育。無駄のない快適な生活を追求。